연락하다:에롤 저우 (씨.)
전화: 플러스 86-551-65523315
모바일/WhatsApp: 플러스 86 17705606359
QQ:196299583
이메일:sales@homesunshinepharma.com
추가하다:230061 중국 허페이시 멍청로 105호 환마오빌딩 1002호
Myovant Sciences는 여성과 남성 치료를 재정의하기 위한 혁신적인 치료법 개발에 중점을 둔 헬스케어 회사입니다. 최근, 회사는 유럽 의약품 기구 (EMA) 인간 사용을위한 의약품위원회 (CHMP)가 승인을 권장하는 긍정적 인 검토 의견을 발표했다고 발표했다.레루골릭스화합물 정제 Ryeqo (relugolix 40 mg, estradiol 1.0 mg, norethindrone acetate 0.5 mg), 약물은 가임기 의 여성의 자궁 근종과 관련된 중등도의 치료를 위해 하루에 한 번 구두로 복용한다. 자궁 근종의 2개의 일반적인 현상은 menorrhagia (HMB) 및 고통입니다.
2020년 3월, 묘반트는 헝가리 게디온 리히터와 독점 라이선스 계약을 체결했다. Gedeon은 유럽, 러시아, 라틴 아메리카, 호주 및 뉴질랜드 및 기타 국가 및 지역에서 relugolix 화합물 정제를 상용화할 것입니다. 자궁 근종 및 자궁 내막증의 치료. 계약 조건에 따르면, Myovant는 레루골릭스 화합물 정제의 글로벌 개발을 이끌고 있으며, Jirui는 지역 임상 개발, 제조 및 해당 지역의 모든 상용화를 담당하고 있습니다.
CHMP의 긍정적인 검토 의견은 3단계 LIBERTY 프로젝트의 안전성과 효과 데이터를 기반으로 합니다. 이 프로젝트에는 2개의 반복된 24주 크로스컨트리 임상 연구(LIBERTY 1 및 LIBERTY 2), 1년 연장 연구, 최대 2년 동안 relugolix 화합물 정제의 안전성과 효과를 평가하기 위한 무작위 철수 연구가 포함됩니다. LIBERTY 1과 LIBERTY 2의 연구 결과는 2021년 2월에 국제 의학 저널 "뉴잉글랜드 의학 저널"(NEJM)에 간행되었습니다. 앞서 언급했듯이, 이 두 연구는 생리손실 완화율의 1차 종점에 도달했고, 동시에 7개의 주요 이차 종점 중 6점에 도달했습니다. Relugolix 화합물 정제 또한 위약에 필적 하는 뼈 미네랄 밀도 유지, 24 주. 잘 용납 내에서 안전의 일부.
LIBERTY 프로젝트의 연구원이자 카탄자로 대학의 부교수인 로버타 벤처렐라 박사는 "가임기 여성의 25% 이상이 자궁 근종으로 고통받고 있습니다. 이 만성 질환쇠약 증상을 일으킬 수 있으며 삶의 질에 상당한 영향을 미칠 수 있습니다. 장기 치료가 필요합니다. 치료 옵션은 제한되어 있으며 많은 여성들이 증상을 완화하기 위해 수술을 받기로 결정합니다. CHMP의 긍정적인 의견은 자궁 근종과 관련되었던 가혹한 생리 출혈 및 고통을 효과적으로 해결하기 위하여 Ryeqo의 잠재력을 또한 검증하고, 중요한 새로운 처리 선택권을 가진 환자와 닥터를 제공할 것입니다."
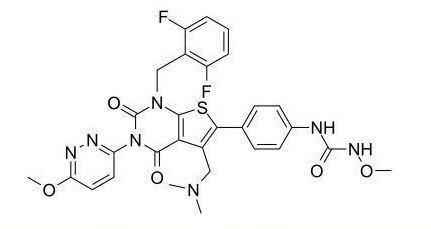
레루골릭스화학 구조 (사진 출처: medchemexpress.com)
현재, relugolix 화합물 정제는 또한 미국 FDA에 의해 검토 되 고, 대상 행동 날짜는 6 월 1, 2021. 승인 된 경우, relugolix 화합물 정제 는 자궁 근종을 가진 여성을위한 하루 치료 계획을 제공 할 것입니다.
2020년 12월, 화이자와 Myovant Sciences는 종양학 및 여성의 건강 분야를 위해 미국과 캐나다에서 relugolix를 개발하고 상용화하기 위해 42억 달러 규모의 협력 협정을 체결했습니다. 화이자는 또한 미국과 캐나다 이외의 종양학에 대한 relugolix를 상용화 할 수있는 독점적 인 권리를 얻을 것이다 (특정 아시아 국가를 제외하고).
Relugolix는 한 번 매일, 구두, 생식샘 방출 호르몬 (GnRH) 뇌 하 수 체에 GnRH 수용 체를 차단 하 고 난소 estradiol의 생산을 줄일 수 있는 수용 체 길 항항제. 이 호르몬은 자궁 근종과 자궁 내막증의 성장을 자극하는 것으로 알려져 있습니다. 또한, relugolix 또한 고환에서 남성 호르몬의 생산을 억제할 수 있습니다., 전립선 암의 성장을 자극할 수 있는.
레루골릭스는 다케다에 의해 개발되었으며, Myovant (로이반트와 다케다에 의해 형성 된 회사)는 일본및 기타 아시아 국가를 제외하고 2016 년 6 월에 독점 글로벌 라이센스를 획득했습니다. 일본에서는 2019년 1월에 Relugolix가 승인되었으며 자궁 근종으로 인한 다음과 같은 증상을 개선하기 위해 Relumina라는 브랜드 이름으로 판매되었습니다: 생리증, 하복부 통증, 요통 및 빈혈.
현재, Myovant는 경구 relugolix 정제를 개발 (120 mg) 고급 전립선 암을 치료 하기 위해 하루에 한 번. 2020년 12월 18일, Orgovyx(relugolix, 120mg 정제)는 미국 FDA의 승인을 받아 전립선암 이진 성인 환자의 치료를 승인받았습니다.
Orgovyx는 고급 전립선 암의 치료를 위해 미국 FDA에 의해 승인 된 최초의 유일한 구두 GnRH 수용체 길항제임을 언급 할 가치가 있다. 약물은 우선 순위 검토 과정을 통해 승인되었다. 3단계 HERO 연구에서, relugolix 치료의 완화율은 96.7%로 높았으며, 이는 류프리데 아세테이트(88.8%)보다 훨씬 높았으며, 주요 심혈관 부작용(MACE)의 위험을 54%까지 감소시키는 것이었습니다.
또한, 묘반은 또한 구강 성 리루골릭스 화합물 정제(relugolix 40mg, estradiol 1.0mg, norethindrone acetate 0.5mg)를 하루에 한 번 개발하여 암컷 자궁 근종 및 자궁내막증을 치료하고 있다. 현재레루골릭스여성 자궁 근종의 치료를위한 화합물 정제는 미국과 EU 규제 기관에 의해 검토되고 있습니다. 자궁내막증 치료를 위한 렐루골릭스 화합물 정제는 2021년 상반기에 마케팅 신청서를 제출할 것으로 예상된다.
1상 연구에서 여성 배란에 대한 레루골릭스 화합물 정제의 100% 억제율을 바탕으로, Myovant와 화이자는 레루골릭스 화합물 정제의 피임 효과를 평가하기 위해 올해 4월에 3상 임상 시험을 시작했습니다.