연락하다:에롤 저우 (씨.)
전화: 플러스 86-551-65523315
모바일/WhatsApp: 플러스 86 17705606359
QQ:196299583
이메일:sales@homesunshinepharma.com
추가하다:230061 중국 허페이시 멍청로 105호 환마오빌딩 1002호
화이자(Pfizer)는 오늘 미국 식품의약국(FDA)이 시빈코(Cibinqo)를 승인했다고 발표했다.아브로시티닙), 성인 환자의 난치성 중등도에서 중증 아토피 피부염(AD) 치료를 위한 1일 1회 경구 JAK1 억제제. 이 약물은 생물학적 제제를 포함한 다른 전신 요법에 대해 부적절한 반응을 받았거나 이러한 요법에 부적절한 난치성 중등도 내지 중증 알츠하이머병 성인을 위해 특별히 표시됩니다. 유럽 연합에서 Cibinqo는 전신 요법에 적합한 중등도에서 중증 AD 성인 환자의 치료를 위해 2021년 12월 승인되었습니다.
복약 측면에서 시빈코의 권장량은 100mg과 200mg이다. 100mg 용량에 반응하지 않는 환자의 경우 200mg 용량을 권장합니다. 또한, 50mg 용량은 다음의 치료에 승인되었습니다. 중등도의 신장애(신부전)가 있는 중등도에서 중증 환자, 또는 사이토크롬 P450(CYP) 2C19 억제제 요법을 받고 있는 환자, 또는 CYP2C19 대사 불량이 알려졌거나 의심되는 AD 성인 환자. 중증 신장애 환자의 경우 1일 1회 50mg의 용량에 반응이 없을 때 1일 1회 100mg을 투여할 수도 있습니다.
Cibinqo is a next-generation oral JAK1 inhibitor developed by Pfizer that has demonstrated safety and efficacy in a large-scale clinical trial program. Cibinqo has also been previously approved in the UK and Japan for the treatment of adolescents and adults with moderate-to-severe AD who are eligible for systemic therapy and have an inadequate response to existing therapies. In the UK and Japan, Cibinqo is approved in doses of 100mg and 200mg.
아토피 피부염(AD)은 피부 염증 및 피부 장벽 결함을 특징으로 하는 만성 피부 질환으로, 피부 홍반, 가려움증, 경화/구진 형성 및 삼출/가피를 특징으로 합니다. 이 질병은 환자와 가족의 일상 생활에 중대한 영향을 미칠 수 있는 심각하고 예측할 수 없으며 종종 쇠약해지는 피부 질환입니다. 많은 중등도에서 중증 환자는 잘 조절되지 않는 질병을 가지고 있으며 그들에게 가장 중요한 증상을 완화하기 위해 추가 치료 옵션이 필요합니다.
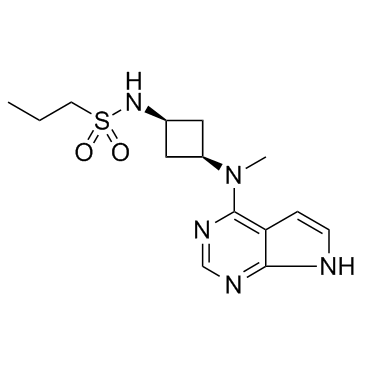
씨빈코& #39;의 유효성분은아브로시티닙, Janus kinase 1(JAK1)을 선택적으로 억제하는 경구용 소분자. JAK1의 억제는 인터루킨(IL)-4, IL-13, IL-31, IL-22 및 흉선 기질 림프구 형성 프라임(TSLP)을 포함하여 아토피 피부염(AD)의 병태생리에 관련된 다중 사이토카인을 조절하는 것으로 생각됩니다.
In September 2021, Cibinqo was approved in the U.K. and Japan for the treatment of adolescent and adult patients with moderate-to-severe atopic dermatitis (AD) aged 12 years and older who are eligible for systemic therapy and have an inadequate response to existing therapies. In December 2021, Cibinqo was approved in the European Union. At present, the marketing application of abrocitinib has been submitted to many countries and regions around the world for review. In the United States, the FDA granted Breakthrough Drug Designation (BTD) to 아브로시티닙2018년 2월 중등도에서 중증 AD의 치료용.